Meldung
Phenole aus Benzoesäuren
Nachrichten aus der Chemie, November 2022, S. 52-55, DOI, PDF. Login für Volltextzugriff.
Von Wiley-VCH zur Verfügung gestellt
Durch eine dem Lossen-Abbau ähnliche Sequenz decarboxylieren Liu und Mitarbeiter Benzoesäuren zu Phenolen. Dazu wandeln sie die Benzoesäure mit meta-Chlorperbenzoesäure (mCPBA) zum gemischten Peroxyanhydrid um. Stöchiometrische Trifluormethansulfonsäure löst eine [1,2]-C-O-Umlagerung aus. Die Reaktion läuft ausschließlich in Dichlormethan und Dichlorethan ab. Als Primärprodukt bildet sich der mCPBA-Ester, aus dem durch Methanolyse das freie Phenol entsteht.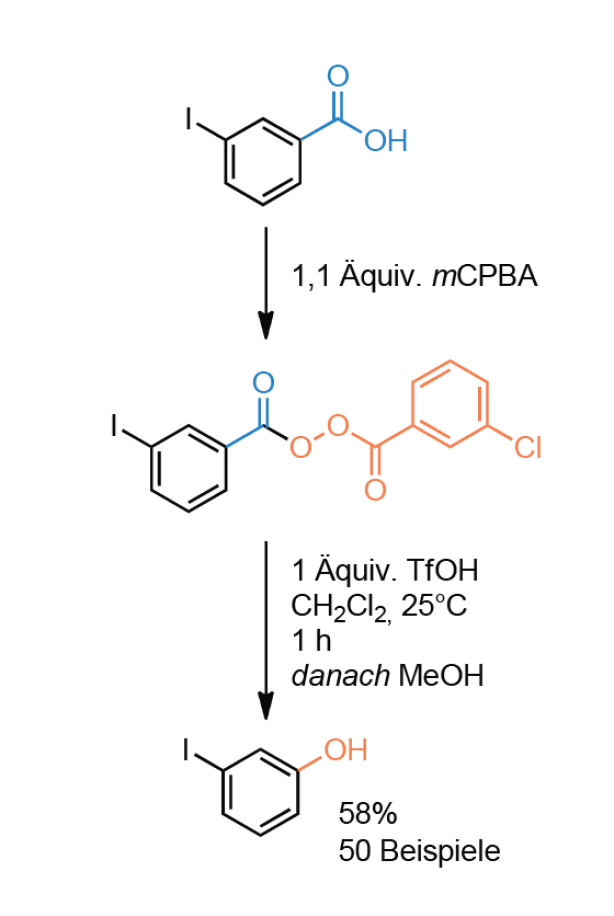
In komplexen Synthesen ermöglicht die Methode, erst den elektronenziehenden Effekt der Carboxylfunktion zu nutzen und später den elektronenliefernden Effekt der Hydroxylgruppe. CCT
- J. Am. Chem. Soc. 2022, 144, 15894
Überprüfung Ihres Anmeldestatus ...
Wenn Sie ein registrierter Benutzer sind, zeigen wir in Kürze den vollständigen Artikel.